

 Задачи с решениями
Задачи с решениями

Элементарная ячейка поваренной соли (NaCl) представляет собой куб, длина ребра которого (постоянная решетки)
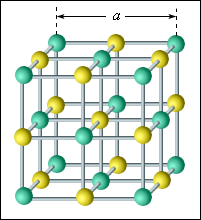 |
| Рисунок 3.6.1.
|
Определим число атомов Na и Cl, входящих в состав одной элементарной ячейки кристалла NaCl. В центре ячейки находится 1 атом Na, полностью принадлежащий этой ячейке. 12 атомов Na находятся на ребрах большого куба, причем каждый из них принадлежит еще трем другим элементарным ячейкам. Следовательно, одной элементарной ячейке принадлежат 4 атома Na:
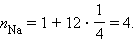
В одной элементарной ячейке кристалла NaCl имеется 6 атомов Cl, находящихся в центрах граней куба, и еще 8 атомов, находящихся в его вершинах. Каждый атом на грани принадлежит еще одной соседней ячейке, а атомы Cl в вершинах куба принадлежат еще 7 ячейкам. Следовательно, одной элементарной ячейке принадлежат 4 атома Cl:
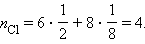
То, что числа атомов Na и Cl в элементарной ячейке совпадают (
Масса
Плотность
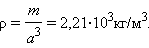
 2 из 2
2 из 2
 |